|
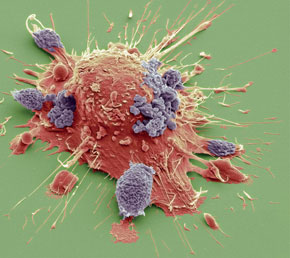
| Células do câncer de boca – microscópio eletrônico de varredura. |
Bombardear um tumor com raios X pode impedir que ele se espalhe pelo corpo. Mas é uma operação delicada.
Mesmo que a radioterapia elimine a maioria das células cancerígenas por danificar o DNA e a induzi-las à morte, as poucas restantes podem sofrer mutações que as tornam imunes aos efeitos da radiação e aumentam sua capacidade de se reproduzir.
Assim, o tumor volta a crescer, mais rápido e mais resistente, e a única opção dos médicos é removê-lo por meio de cirurgia. No caso do câncer de cabeça e pescoço, no entanto, esse último recurso é muitas vezes mutilador. Ele prejudica a estética, a deglutição, a fala e até mesmo a respiração.
Buscando um modo mais eficiente de combater esse tipo de tumor, uma equipe multidisciplinar de 18 pesquisadores de Minas Gerais e de São Paulo desenvolveu uma estratégia promissora para tornar as células tumorais mais sensíveis à radiação. Publicados em maio deste ano no Journal of Cancer Science and Therapy, os resultados da pesquisa, ainda em fase pré-clínica, sugerem que a radioterapia, acompanhada de um procedimento que impede a livre circulação de íons de cálcio no núcleo das células pode reduzir pela metade o tempo de exposição à radiação e diminuir drasticamente o risco de reincidência do tumor.
Sob a supervisão da bióloga celular Maria de Fátima Leite, da Universidade Federal de Minas Gerais (UFMG), e do imunologista Olindo Assis Martins Filho, do Centro de Pesquisas René Rachou, da Fundação Oswaldo Cruz em Belo Horizonte, a pesquisadora Lídia Maria Andrade concebeu essa estratégia. Quando ainda era estudante de odontologia, Lídia teve a oportunidade de acompanhar de perto o sofrimento de pacientes com câncer de cabeça e pescoço. Provocado principalmente pelo fumo e pelo consumo de álcool, ele é a oitava maior causa de morte por câncer no mundo. Só o câncer na cavidade oral deve atingir mais de 14 mil pessoas este ano no Brasil, estima o Instituto Nacional do Câncer. O médico João Victor Salvajoli, especialista em radioterapia do Hospital Alemão Oswaldo Cruz, em São Paulo, explica que no tratamento do câncer de cabeça e pescoço a radioterapia é geralmente aliada a uma quimioterapia com substâncias que deixam as células mais sensíveis à radiação. Os efeitos colaterais são uma série de lesões na pele e na mucosa que podem afetar gravemente a deglutição, o paladar e a salivação. Além disso, há um alto risco de recidiva da doença.
Em 2008, interessada em descobrir algo que pudesse diminuir ainda mais a resistência das células do câncer de cabeça e pescoço à radiação, Lídia procurou Maria de Fátima, cujas pesquisas na última década se concentraram no estudo do papel que os íons de cálcio do núcleo celular desempenham na multiplicação de tumores. As pesquisadoras decidiram então investigar se o tamponamento do fluxo de cálcio nuclear diminuiria a resistência à radiação dessas células.
Canais bloqueados
Os íons de cálcio são peças fundamentais da maquinaria que faz funcionar as células. A concentração maior ou menor de cálcio dispara ou suprime uma série de processos vitais, como a ativação de genes. Dentro das células há uma organela com vários compartimentos que armazenam os íons de cálcio e é conhecida pelo nome de retículo endoplasmático. As paredes desse retículo são repletas de proteínas, entre as quais algumas funcionam como canais. São os chamados canais de cálcio, que permanecem fechados a maior parte do tempo e só se abrem, deixando o íon sair para o citoplasma, quando uma substância específica, o inositol trifosfato, se liga a eles. Passada a necessidade, os íons de cálcio são bombeados de volta ao interior do retículo.
Em 2003, em colaboração com pesquisadores das Universidades de Cornell e Yale, nos Estados Unidos, Maria de Fátima descreveu em um artigo na revista Nature Cell Biology como o cálcio do núcleo celular é controlado de maneira independente do cálcio localizado no restante da célula. No núcleo há outro reservatório desses íons, chamado de retículo nucleoplasmático. Em 2007, com seus colegas de Yale, a pesquisadora publicou um trabalho no Journal of Biological Chemistry demonstrando que bloquear a saída de 70% do cálcio do retículo nucleoplasmático reduzia a reprodução das células de um tumor de fígado implantado em camundongos. “O tumor cresceu absurdamente menos que o normal”, lembra a pesquisadora. “Sabe-se, há muito tempo, que o cálcio participa das diferentes fases de multiplicação das células, o chamado ciclo celular”, explica. “O bloqueio do cálcio interrompe o ciclo celular e, assim, a célula não consegue se dividir.”
Tanto no tumor de fígado quanto agora nas células de câncer de cabeça e pescoço cultivadas em laboratório o bloqueio do cálcio foi obtido por meio de uma técnica de engenharia genética. Com o auxílio de um adenovírus artificial, os pesquisadores induziram as células tumorais a produzirem dentro do núcleo uma proteína que imita a parte dos canais de cálcio que se liga ao inositol trifosfato. Com quase todo o inositol trifosfato neutralizado por essas proteínas, a maioria dos verdadeiros canais de cálcio do retículo nucleoplasmático permanece fechada (ver infográfico acima). Sem a quantidade necessária de cálcio, as células tumorais diminuem sua capacidade de reprodução.
 Esse procedimento proporcionou uma vantagem adicional. O bloqueio do cálcio reduziu apenas a proliferação das células tumorais. Células saudáveis de gengiva, quando submetidas à terapia gênica, continuaram a se reproduzir normalmente. Segundo os pesquisadores, as células saudáveis demonstraram ser menos sensíveis à retenção do cálcio nuclear. Essa constatação sugere que uma terapia baseada nessa estratégia poderia não danificar os tecidos saudáveis em volta do tumor.
Esse procedimento proporcionou uma vantagem adicional. O bloqueio do cálcio reduziu apenas a proliferação das células tumorais. Células saudáveis de gengiva, quando submetidas à terapia gênica, continuaram a se reproduzir normalmente. Segundo os pesquisadores, as células saudáveis demonstraram ser menos sensíveis à retenção do cálcio nuclear. Essa constatação sugere que uma terapia baseada nessa estratégia poderia não danificar os tecidos saudáveis em volta do tumor.
Teste realista
Nos testes, Lídia e a equipe do físico Jony Marques Geraldo, do Instituto de Radioterapia São Francisco, em Belo Horizonte, irradiaram com raios X as culturas de células tomando cuidado para que cada uma delas recebesse a mesma quantidade de radiação – o experimento poderia chegar a resultados equivocados caso algumas células recebessem mais ou menos radiação do que as outras. Houve também o cuidado de tentar reproduzir as condições reais de uma radioterapia em seres humanos, um esforço, segundo os pesquisadores, inédito em pesquisas in vitro. A irradiação foi realizada em sessões diárias, com a mesma máquina de radioterapia usada em pacientes com câncer, com os frascos das culturas de células dentro de uma plataforma de acrílico de água, que imitava um corpo humano com tumores. “Nossa preocupação foi chegar o mais próximo possível da situação clínica”, diz Lídia.
 O resultado da combinação das terapias foi bastante encorajador. Os pesquisadores observaram nas células tratadas uma redução dos níveis de duas proteínas: a ADAM17 e a EFGR, associadas à resistência à radiação. Mais importante ainda, houve um decréscimo de mais de 90% na formação de novas colônias de células tumorais após o tratamento conjunto. Comparada ao grupo de controle, a radioterapia sozinha reduziu em 36% a formação de colônias. Mesmo com o uso de aproximadamente metade da dose padrão de radiação, a probabilidade de sobrevida do tumor permaneceu baixa. Isso sinaliza que o emprego conjunto da radioterapia e da proteína que bloqueia o cálcio no núcleo das células de câncer poderia combater o tumor de modo mais eficiente, expondo menos o paciente aos danos do tratamento padrão.
O resultado da combinação das terapias foi bastante encorajador. Os pesquisadores observaram nas células tratadas uma redução dos níveis de duas proteínas: a ADAM17 e a EFGR, associadas à resistência à radiação. Mais importante ainda, houve um decréscimo de mais de 90% na formação de novas colônias de células tumorais após o tratamento conjunto. Comparada ao grupo de controle, a radioterapia sozinha reduziu em 36% a formação de colônias. Mesmo com o uso de aproximadamente metade da dose padrão de radiação, a probabilidade de sobrevida do tumor permaneceu baixa. Isso sinaliza que o emprego conjunto da radioterapia e da proteína que bloqueia o cálcio no núcleo das células de câncer poderia combater o tumor de modo mais eficiente, expondo menos o paciente aos danos do tratamento padrão.
“É uma prova de conceito bastante elegante”, comenta o oncologista Roger Chammas, da Universidade de São Paulo. Ele ainda ressalta que, apesar de o estudo ter utilizado células de câncer de cabeça e pescoço, a terapia proposta poderia ser aplicada, em princípio, a outros tipos de câncer resistentes à radioterapia. Helena Segretto, oncologista especialista em radiobiologia da Universidade Federal de São Paulo (Unifesp), nota que a radioterapia associada ao bloqueio de cálcio paralisou o processo de divisão das células tumorais justamente nas fases em que elas são mais sensíveis à radiação, induzindo um aumento da morte celular. “A melhora da resposta das células tumorais à radiação é o grande desejo dos médicos radioterapeutas”, afirma.
Todos os especialistas, entretanto, concordam que ainda há um longo caminho pela frente até se provar a viabilidade dessa estratégia. Helena afirma que, antes dos primeiros testes com seres humanos, serão necessários experimentos com animais de laboratório, nos quais as células tumorais interagem com as sadias, para se ter certeza de que as últimas realmente não serão afetadas pela terapia. “Os primeiros testes com animais já começaram e as parcerias para futuros ensaios com equipes do Hospital das Clínicas da UFMG já estão em andamento”, diz Maria de Fátima.
————
Artigos científicos
ANDRADE, L.M. et al. Nucleoplasmic calcium buffering sensitizes human squamous cell carcinoma to anticancer therapy. Journal of Cancer Science and Therapy. 25 mai. 2012.
RODRIGUES, M.A. et al. Nucleoplasmic calcium is required for cell proliferation. The Journal of Biological Chemistry. v. 282. 8 jun. 2007.